Xem toàn bộ tài liệu Lớp 9: tại đây
Giải Bài Tập Hóa Học 9 – Bài 8 : Một số bazơ quan trọng giúp HS giải bài tập, cung ứng cho những em một mạng lưới hệ thống kiến thức và kỹ năng và hình thành thói quen học tập thao tác khoa học, làm nền tảng cho việc tăng trưởng năng lượng nhận thức, năng lượng hành vi :
Bài 1: Có 3 lọ không nhãn, mỗi lọ đựng một chất rắn sau: NaOH, Ba(OH)2, NaCl. Hãy trình bày cách nhận biết chất đựng trong mỗi lọ bằng phương pháp hóa học. Viết các phương trình hóa học nếu có.
Lời giải:
Bạn đang đọc: Bài 8: Một số bazơ quan trọng
Lấy mẫu thử từng chất và đánh số thứ tự. Hòa tan những mẫu thử vào H2O rồi thử những dung dịch :
– Dùng quỳ tím cho vào từng mẫu thử
+ Mẫu nào làm quỳ tím hóa xanh đó là NaOH và Ba ( OH ) 2 .
+ Còn lại là NaCl không có hiện tượng kỳ lạ .
– Cho H2SO4 vào những mẫu thử NaOH và Ba ( OH ) 2
+ Mẫu nào có kết tủa trắng đó là loại sản phẩm của Ba ( OH ) 2
PTHH : Ba ( OH ) 2 + H2SO4 → BaSO4 ↓ trắng + 2H2 O
+ Còn lại là NaOH .
Bài 2: Có những chất sau: Zn, Zn(OH)2, NaOH, Fe(OH)3, CuSO4, NaCl, HCl. Hãy chọn những chất thích hợp điền vào sơ đồ phản ứng sau và lập phương trình hóa học.
a) … → Fe2O3 + H2O
b) H2SO4 + … → Na2SO4 + H2
c) H2SO4 + … → ZnSO4 + H2O
d) NaOH + … → NaCl + H2O
e) … + CO2 → Na2CO3 + H2O.
Lời giải:
a) 2Fe(OH)3 → Fe2O3 + 3H2O
b) H2SO4 + 2NaOH → Na2SO4 + 2H2O
c) H2SO4 + Zn(OH)2 → ZnSO4 + 2H2O
d) NaOH + HCl → NaCl + H2O
e) 2NaOH + CO2 → Na2CO3 + H2O.
Bài 3: Dẫn từ từ 1,568 lít khí CO2(đktc) vào một dung dịch có hòa tan 6,4g NaOH.
a) Chất nào đã lấy dư và dư là bao nhiêu (lít hoặc gam)?
b) Hãy xác định muối thu được sau phản ứng.
Lời giải:
a ) Trước tiên ta phải xem muối nào được tạo thành ( NaHCO3 hay Na2CO3 ) .
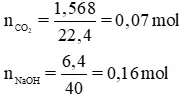
nNaOH > 2 nCO2 nên muối sau phản ứng là Na2CO3 ; CO2 phản ứng hết, NaOH dư .
Phương trình hóa học của phản ứng :
2N aOH + CO2 → Na2CO3 + H2O
Theo pt nNaOH pư = 2. nCO2 = 2. 0,07 = 0,14 mol ⇒ nNaOH dư = 0,16 – 0,14 = 0,02 mol
Khối lượng chất dư sau phản ứng :
mNaOH = 0,02. 40 = 0,8 g .
b ) Theo pt nNa2CO3 = nCO2 = 0,07 mol
⇒ m Na2CO3 = 0,07 x 106 = 7,42 g .
(Lưu ý cách xác định sản phẩm muối tạo thành sau phản ứng:
Đặt tỉ lệ 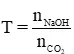
Nếu T ≥ 2 ⇒ Chỉ tạo muối Na2CO3 ; Khi T = 2 phản ứng vừa đủ, T > 2 NaOH dư
Nếu T ≤ 1 ⇒ Chỉ tạo muối NaHCO3 ; Khi T = 2 phản ứng vừa đủ, T < 1 CO2 dư
Nếu 1 < T < 2 ⇒ Tạo cả 2 muối
Bài 1: Viết các phương trình hóa học thực hiện các chuyển đổi hóa học sau:
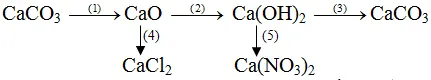
Lời giải:
Phương trình hóa học của những phản ứng :
(1) CaCO3
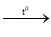 CaO + CO2
CaO + CO2
CaO + CO
(2) CaO + H2O → Ca(OH)2
(3) Ca(OH)2 + CO2 → CaCO3 + H2O
(4) CaO + 2HCl → CaCl2 + H2O
(5) Ca(OH)2 + 2HNO3 → Ca(NO3)2 + 2H2O
Các bài Giải bài tập | Để học tốt Hóa học 9 Bài 8: Một số bazơ quan trọng
Bài 2: Có ba lọ không nhãn, mỗi lọ đựng một trong ba chất rắn màu trắng sau: CaCO3, Ca(OH)2, CaO. Hãy nhận biết chất đựng trong mỗi lọ bằng phương pháp hóa học. Viết phương trình hóa học.
Lời giải:
Lấy mỗi chất rắn 1 ít làm mẫu thử và đánh số thứ tự
– Cho ba chất rắn vào nước :
+ Chất nào không tan trong nước đó là CaCO3 .
+ Chất nào phản ứng với nước làm nóng ống nghiệm là CaO
PTHH : CaO + H2O → Ca ( OH ) 2
+ Chất chỉ tan 1 phần tạo chất lỏng màu trắng và có 1 phần kết tủa lắng dưới đáy là Ca ( OH ) 2
Các bài Giải bài tập | Để học tốt Hóa học 9 Bài 8: Một số bazơ quan trọng
Bài 3: Hãy viết các phương trình hóa học khi cho dung dịch NaOH tác dụng với dung dịch H2SO4 tạo ra:
a ) Muối natri hiđrosunfat .
b ) Muối natri sunfat .
Lời giải:
a ) Muối natri hidrosunfat : NaHSO4
H2SO4 + NaOH → NaHSO4 + H2O
b ) Muối natri sunfat : Na2SO4
H2SO4 + 2N aOH → Na2SO4 + 2H2 O
Các bài Giải bài tập | Để học tốt Hóa học 9 Bài 8: Một số bazơ quan trọng
Bài 4: Một dung dịch bão hòa khí CO2 trong nước có pH = 4. Hãy giải thích và viết phương trình hóa học của CO2 với nước.
Lời giải:
Dung dịch bão hòa CO2 trong nước tạo ra dung dịch axit cacbonic ( H2CO3 ) là axit yếu, có pH = 4 .
CO2 + H2O ⇌ H2CO3 .
Các bài Giải bài tập | Để học tốt Hóa học 9 Bài 8: Một số bazơ quan trọng
Source: https://expgg.vn
Category: Thông tin









